DETERMINACIÓN DEL PODER BACTERICIDA DE LOS POUMEROS DERJVADOS DEL TETRAMETIL ETILEN AMONIO EN AGUAS CON DIFERENTES
DEMANDAS BIOQUÍMICAS DE OXÍGENO
 Liliana Morales y Martha Mustre
Liliana Morales y Martha Mustre
EscueLa de Cie'1das QulmJCa, UoiVersidad La Salle
RESUMEN
El objetivo de este trabajo fue determinar si los polímeros derivados del tetrametil etilen amonio segulan actuando como bactericidas y/o
bacteriostáticos sobre Escherichia coli y Streptococcus faecalis en presencia de diferentes cantidades de materia
orgánica. A 900 mg/I de DBO 400 ppm de los polímeros derivados del tetrametil etilen amonio siguen siendo efectivos como bactericidas y/o
bacteriostáticos. Se pudo observar que el Streptococcus faecalis es más resistente que el Escherichía coli en presencia de materia
orgánica.
INTRODUCCIÓN
En la actualidad, lo estricto y riguroso de las regulaciones ambientales obligan a las industrias de todo tipo, a usar el agua de un modo más eficiente
y a implementar tratamientos para las aguas de desecho que producen (3,5).
Algunas compañlas han comprendido que utilizando la tecnologia química disponible pueden resolver sus problemas de obtención de agua. Han observado que
el agua usada en un proceso puede ser nuevamente uilizada en otro, donde la calidad del agua no sea tan estricta y, que aún después de esto, ser
convenientemente tratada para poder ser utilizada como agua de riego, con la limitante de que no sea para terrenos agricolas (11, 12, 14).
Los efluentes industriales pueden originar grandes problemas. La variedad de los productos que se vierten, tóxicos o consumidores de oxígeno, requiere
una investigación propia en cada tipo de industria y el empleo de procesos de tratamiento específicos (14, 15).
Los procesos de tratamiento pueden ser flsicos. qulmicos o biológicos e incluyen técnicas de:
- Sedimentación
- Neutralización
- Precipitación
- Floculación y decantación
- Desgasificación
La mayoría de estos procesos se usan de forma combinada y de forma simultánea para obtener mejores resultados (17).
Las impurezas del agua varían en tamafío; la eliminación de una gran proporción de éstas, se lleva a cabo por sedimentación. en el tíatamiento del agua
residual. sin embargo. debido a que muchas de las impurezas son demasiado pequelias para obtener un proceso de eliminación eficiente por sedimentación
basado sólo en la gravedad, es preciso llevar a cabo la combinación de estas particulas en agregados de mayor tamaño y más fácilmente decantables, con
el fin de obtener una separación satisfactoria por sedimentación. Este proceso se llama floculación (17, 19).
Para poder llevar a cabo la floculación se utilizan productos químicos desde sales hasta pollmeros, dentro de estos últimos encontramos una gran
variedad, ya sea orgánicos o inorgánicos. Los más usados son los polielectrolitos que contienen aminas o compuestos cuaternarios de amonio en su
formulación, lo

/,,..\,
que les confiere carácter alguicida y bactericida y, al combinarse con otras moléculas, funcionan como antiespumante y floculante (2).
Se ha observado que la eficiencia de un agente de floculación depende de varias características, entre las que se encuentra la cantidad de materia
orgánica y microorganismos presentes en el agua. Un parámetro de la primera variable. es la demanda bioquímica de oxígeno. que indica la cantidad de
oxígeno necesario para degradar la materia orgánica presente en dicha agua, por lo tanto. es un indicador del grado de contaminación de agua residual o
industrial (21, 22).
METOOOLOGIA
La cepas de Escherichia colí y Streptococcus faecalis fueron donadas por el Laboratorio de Microbiología de la Universidad La Salle y
se resembraron cada semana en cajas con agar BHI. para tener un cultivo viable y obtener el inóculo necesario para realizar las curvas de crecimiento y
determinar el poder bactericida del polímero.
El polímero utilizado fue el: Oicloruro de Poli (oxietilen (dimetil iminio)etilen (dirnetil iminio) etileno), el cual se obtuvo a partir de una
síntesis realizada en el Instituto de Química de la UNAM. proporcionado en solución acuosa muy viscosa, por lo que para manejar la concentración
requerida, se liofilizó el polímero, para manejar cantidades exactas al eliminar toda el agua (18)
Curvas de crecimiento
Se calcularon las cuNas de crecimiento de E. colí y Stp. faecalis en el nefelómetro de Mac Farlan, bajo diferentes concetraciones de
080 (100, 300 o 900 mg/I) determinadas según la norma NOM-AA-28-1981 (1,2). Las soluciones que se utilizaron se prepararon utilizando piloncillo como
materia orgánica. Las lecturas tomadas para determinar el inóculo de bacteria se presentan en la siguiente tabla:
Longitud de onda Densidad óptica
600 nm
650 nm
0.267 - 0.360
0.227 - 0.347
Para conocer el número de microorganismos viables se suspendió un cultivo joven de cada cepa en agua destilada. Se ajustó la turbidez a la del tubo No.
1 del nefelómetro. El número de microorganismos viables se determinó por la técnica de vaciado en placa.
Oetenninación del poder bactericida del polímero
El poder bactericida del polímero se determinó por su capacidad para reducir el crecimiento de la bacteria en soluciones con 100, 300 o 900 DBO. Las
bacterias se incubaron con las soluciones de melaza, y una vez alcanzada la fase de crecimiento logarítmico se cultivaron en presencia de 20 mi de una
solución del polímero (concentrción final de 400 ppm). Se sembraron alícuotas de 0.5 mi en placas. y la reducción en el crecimiento se calculó por
comparación con una muestra que no había sido cultivada con el polímero.
ANÁLISIS DE RESULTADOS
Se determino que los DBO's a utilizar serían los de 100. 300 y 900 mg/I: siendo los dos primeros los rangos entre los cuales se encuentran las normas
técnicas ecológicas para las industrias alimenticias. La última concentración se utilizó para observar la eficiencia del polímero.
Es importante recordar que para cada tipo de agua varía la concentración del pollmero. por lo que es necesario hacer los "jar test'' en cada caso.

 La cantidad de melaza necesaria para obtener los DBO's de 100, 300 y 900 mg/I, no guarda una relación lineal, esto se observa durante la determinación
de los gramos necesarios de melaza, ya que si lo obtenlamos haciendo una regla de 3, el DBO obtenido era mucho mayor al deseado.
La cantidad de melaza necesaria para obtener los DBO's de 100, 300 y 900 mg/I, no guarda una relación lineal, esto se observa durante la determinación
de los gramos necesarios de melaza, ya que si lo obtenlamos haciendo una regla de 3, el DBO obtenido era mucho mayor al deseado.
La determinación del DBO es simple, sin embargo la norma oficial Mexicana no toma en cuenta varios parámetros, que la literatura si reporta que hacen
más sencilla y exacta la determinación del mismo (9).
TiMl>o(ln)
 -100 nvi i
-100 nvi i
--O- :.xinV'I 1
----900 nV'I 1

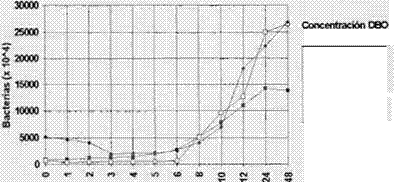
Los diferentes tiempos de adaptación de Escheríchía coli y Streptococcus faecalís a los distintos DBO's se deben
principalmente a la diferente presión osmótica (concentración de azúcar) que el medio presenta dependiendo del 080 del cual se trate y está
directamente relacionada con la capacidad de adaptación de cada microorganismo a dicho medio. Las curvas de crecimiento de estas bacterias se muestran
en las figuras 1 y 2.
 Es por eso, que si se comparan los datos obtenidos en una solución sin miel y otra con miel se obseNa que la cantidad de microorganismos disminuye y
que, conforme transcurre el tiempo vuelve a aumentar.
Es por eso, que si se comparan los datos obtenidos en una solución sin miel y otra con miel se obseNa que la cantidad de microorganismos disminuye y
que, conforme transcurre el tiempo vuelve a aumentar.
Debido al comportamiento anterior. se determinó que para tener condiciones más representativas de las naturales, en el momento de agregar el polímero,
se esperaría hasta que el microorganismo se encontrara en su fase logarítmica de crecimiento.
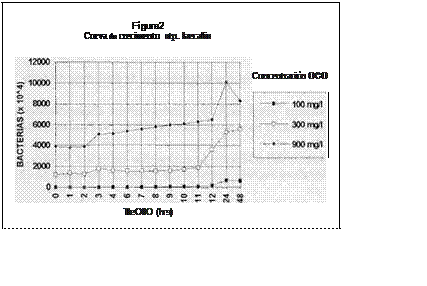
 Para ambos microorganismos se observa que la máxima eficiencia se obtuvo en un rango máximo de 30 rnin (figura 3 y 4), a excepción de Escheríchia colí con 300 mg/I de 080 en donde la máxima eficiencia se obtuvo a las 5 hr (figura 3). Sin embargo, es de hacerse notar que se
presenta una buena eficiencia a 1 min de 96.71%, a 30 min de 95.33% y a 1 hr. de 97.16%, por lo que para fines prácticos podernos tomar cualquiera de
los dos últimos datos como el ideal para continuar el tratamiento de agua; pues la
Para ambos microorganismos se observa que la máxima eficiencia se obtuvo en un rango máximo de 30 rnin (figura 3 y 4), a excepción de Escheríchia colí con 300 mg/I de 080 en donde la máxima eficiencia se obtuvo a las 5 hr (figura 3). Sin embargo, es de hacerse notar que se
presenta una buena eficiencia a 1 min de 96.71%, a 30 min de 95.33% y a 1 hr. de 97.16%, por lo que para fines prácticos podernos tomar cualquiera de
los dos últimos datos como el ideal para continuar el tratamiento de agua; pues la
literatura reporta que para que el tratamiento utilizando coagulación y floculación sea aplicable no debe tardar más de 4 hr, siendo el ideal de 2
hr.máximo.

 135
135
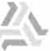
!60.00'll. .•.
40,00%
io.00% 1
figura.4
Cur
•
.a
1
con
pollnt•
ro
pan
.
$Cp
.
f.Hc.alo
·
Conu
nll>ctón
080
- • tOO mg/I
---•
-
too
mg/I
Es importante recordar que las condiciones de aplicación del pollmero, sobre todo su disolución en el medio. son de suma importancia para obtener la
máxima eficiencia.
 El porcíento de reducción de las bacterias se ve afectado por varios factores: La acción bactericida del polímero, la poca disponibilidad de materia
orgánica conforme
El porcíento de reducción de las bacterias se ve afectado por varios factores: La acción bactericida del polímero, la poca disponibilidad de materia
orgánica conforme
o.on.
1-
-
2
g
! •
T
i
a«tp&
(
min
)
transcurre el tiempo para las bacterias que
todav ía son viables, el ciclo natural de crecimiento de las mismas.
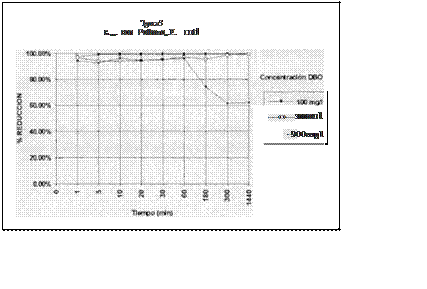
En las figuras 3 y 4 donde se obseiva un descenso en el porciento de reducción, nos hace pensar que las bacterias viables,continúan reporduciéndose
aprovechando la materia orgánica todavía disponible,esto último se obseiva en el caso del Streptococcus faecalis por lo que podemos decir que
el Streptococcus faecalis es más resistente que la Escherichia colí cuando hay materia orgánica.
En todos los casos, donde en la última toma (24 hr). el porciento de reducción aumenta debe tomarse en cuenta el ciclo natural de desarrollo del
microorganismo, así como que se trata de un sistema cerrado.
CONCLUSIONES
La Norma Oficial Mexicana debe modificarse , agregándosele los parámetros que la literatura reporta.
El tiempo de adaptación a la mezcla agua-melaza varía con la concentración dependiendo del microorganismo. El Streptococcus faecalis presenta
un mayor tiempo de adaptación que la Escherichía co/í.
El tiempo necesario para obtener la máxima eficiencia del polimero se encuentra entre los 1O min. y 30 min., quedando dentro del rango de 2 hr que ta
literatura reporta como viable para un tratamiento (11).
La Escheríchía cofi es menos resistente a la acción bactericida del polf mero que el Streptoco ccus faecalis.
Aplicando correctamente el polímero, la eficiencia del mismo a altas concentraciones de 080, es de más del 90% como promedio.
A 400 ppm el polímero además de actuar como floculante y coagulante es bactericida frente a
Escherichia coli
y Streptococcus faecalis.
No hay una DBO que inactiva al polímero como agente bactericida, ya que basta con modificar la cantidad de polimero de acuerdo con el 080.
El uso del po!lmero disminuye el uso de otros agentes desinfectantes en aguas tratadas, al disminuir en un solo proceso no sólo la materia orgánica
sino también los microorganismos.

REFERENCIAS
1.- Aguas- determinación de oxígeno disuelto, Norma Oficial MeX"icana, NOM-AA-12-1980. Dirección General de Normas.
2.- Análisis de agua- determinación de la demanda bioquímica de oxígeno , Norma Oficial
Mexicana, NOM-AA-18-1981 , Dirección General de Normas.
3.- Benarde A . Melvin, Our precarious habitat. fifteen years later, Ed. John Wiley and Sons.,USA 1989.
4.- Butterfield Wattie E. and Chamber C.W.. Bactericida! efeci ency of quaternarv ammonium compounds , Public Health. Rep. 1949, pp. 64 .
5.- Calatayud Eva, "La industria de tratamiento de agua: estrategias para el ahorro y rehuso de la industria", en: Estrategia i ndustrial, Julio 1993, No. 115, Año X, ED. Cideti. México 1993.
6.- Conell Des W.. Miller Gregory J., "Chemistry and ecotoxicology of pollution", en: Environmental science and technology, (a
Wiley-lnterscience series of texts and monographs). ED. John Wiley and Sons., USA 1984, pp. 75-124.
7.-Oegremont ,Manual técnico del agua, 4 edición,1979, pp: 29-33,76-79,116-121,304-305.622-628,674-
683,741-749 ,930-93 3.
8.- Oeming H.G., El agua: un recurso insustituible, ED. Nuevo Mar, 1979.
9.- Diaz de Santos, Métodos normalizados para el análisis de aguas potables y residuales , ED. ALPHA AWWA-WPCF , 1992. pp.
4-162 a 5-15.
1O.- Dugan Patrick R., Biochemical ecology of water pollution, ED. Plenum Press. USA 1972,pp. 3-9,33- 39.
11.- Eckenfelder Wesley W.,"Industrialwater pollution control", McGraw-Hillseries en: Water Resources and Enviromental Enqin
eering, ED. McGraw-Hill, USA 1991, pp. 1-11O.
12.- Eskel, Nordell, Kendel. Tratamiento de agua para la industria y otros usos. Compañia Editorial Continental S.A. 1961, pp. 123-131,168-172,176,177.
13.- Kemmer Frank N. (Ed.), The nalco water handbook. Ed. Me Graw-Hill lnternational Editions, Chemical Engineering series, 2 nd. edition, USA 1988,
pp. 8.3 A 8.22 .
14.- Lund Herbert F. Manual para el control de la contaminación industrial, ED. Instituto de estudios de administración local, España, 1974, pp.
534-561.
15.- Parkinson Gerald, Basta Nicholas, Water supply and disposal uptade. Chemical Engineering, April 1991.
16.- Recursos mundiales (1992-1992). una qufa para el ambiente mundia l . hacia el desarrollo sustentable , Banco Interamericano de Desarrollo, ED. Oxford University Press, USA 1992,
pp. 185-203.
17.- Rigola Lapeña Miguel,Tratamiento de aguas industriales:aguas de proceso y residuales, Productica (colección) , EO. Marcombo Boixarbu Editores
S.A., España 1989, pp. 27-71, 137-156 .

18.- Rodríguez Aguilar Hector Manuel, Obtención de polímeros derivados de sales cuaternarias de amoni o. Tesis. Universidad La Salle, México 1992.
19.- Sheppard T. Powel1, Acondicionami ento de aguas para l a i ndustri a,ED Limusa. Mé:t:ico 1986. pp.
35-75.
20.- Standard methods for t he exami nal i on of water and waste water, ED. American Public Heatth Association lnc., 12 th edition, USA 1965, pp.
414-511 .
21 .- Turkman A, Dokuz Eylül University , Dept. of Enviromental Engineering, lzmir-Turkey, "Polymer application examples in industrialwastewater treatment"
en: New developmentes i n i ndustrial waste water treatment, Aysen Turkman and Orhan Uslu (Ed.), Nato Así series.
Series E: Applied Sciences vol. 191, EO· Kluwer Academic Publishers.. USA 1989, pp. 93-109.
22.- Uslu Orhan, Dr-lng. (prof), Efluent water quality requirernents, Dokuz EylOI Uníversity, Dept. of Environmenta l Engineering, 31200 Bornova
-lzmir,Turkey , en: New developrnents in industrial waste water treatment. Aysen Turkman and Orhan Uslu (Ed), Nato series, Series E: Applied sciences Vol. 191.. ED. Kluwer Academic Publishers.. USA 1989, pp. 1-10.
23.- Walter J., Weber Jr., Control de la calidad del agua , procesos fisicoguímicos,ED. Reverte, España
1979, pp. 64-66, 78,84-94.
24 .- Water qualitv and treatment , ( A Handbook of comuníty watter supplies). American water works associatíon, 4 th edición, USA,1990, pp.
100-105,269-273,280-295 .300-309 , 322-329,334-335, 342-343,
358-367 .
25.- White Clifford, Geo. Desinfection of waste-water and water reuse, ED. Van Nostrand Reinhold Environmental
Engineering Series, 1978. pp. 11-25.
![]() Liliana Morales y Martha Mustre
Liliana Morales y Martha Mustre
![]()
 La cantidad de melaza necesaria para obtener los DBO's de 100, 300 y 900 mg/I, no guarda una relación lineal, esto se observa durante la determinación
de los gramos necesarios de melaza, ya que si lo obtenlamos haciendo una regla de 3, el DBO obtenido era mucho mayor al deseado.
La cantidad de melaza necesaria para obtener los DBO's de 100, 300 y 900 mg/I, no guarda una relación lineal, esto se observa durante la determinación
de los gramos necesarios de melaza, ya que si lo obtenlamos haciendo una regla de 3, el DBO obtenido era mucho mayor al deseado.
 -100 nvi i
-100 nvi i
 Es por eso, que si se comparan los datos obtenidos en una solución sin miel y otra con miel se obseNa que la cantidad de microorganismos disminuye y
que, conforme transcurre el tiempo vuelve a aumentar.
Es por eso, que si se comparan los datos obtenidos en una solución sin miel y otra con miel se obseNa que la cantidad de microorganismos disminuye y
que, conforme transcurre el tiempo vuelve a aumentar.
 Para ambos microorganismos se observa que la máxima eficiencia se obtuvo en un rango máximo de 30 rnin (figura 3 y 4), a excepción de Escheríchia colí con 300 mg/I de 080 en donde la máxima eficiencia se obtuvo a las 5 hr (figura 3). Sin embargo, es de hacerse notar que se
presenta una buena eficiencia a 1 min de 96.71%, a 30 min de 95.33% y a 1 hr. de 97.16%, por lo que para fines prácticos podernos tomar cualquiera de
los dos últimos datos como el ideal para continuar el tratamiento de agua; pues la
Para ambos microorganismos se observa que la máxima eficiencia se obtuvo en un rango máximo de 30 rnin (figura 3 y 4), a excepción de Escheríchia colí con 300 mg/I de 080 en donde la máxima eficiencia se obtuvo a las 5 hr (figura 3). Sin embargo, es de hacerse notar que se
presenta una buena eficiencia a 1 min de 96.71%, a 30 min de 95.33% y a 1 hr. de 97.16%, por lo que para fines prácticos podernos tomar cualquiera de
los dos últimos datos como el ideal para continuar el tratamiento de agua; pues la
 El porcíento de reducción de las bacterias se ve afectado por varios factores: La acción bactericida del polímero, la poca disponibilidad de materia
orgánica conforme
El porcíento de reducción de las bacterias se ve afectado por varios factores: La acción bactericida del polímero, la poca disponibilidad de materia
orgánica conforme