Introducción
A finales del año 2019 se registró un aumento en la incidencia de pacientes con infección respiratoria, descubriéndose la presencia de un nuevo coronavirus, clasificándose como Síndrome Respiratorio Agudo Severo por coronavirus tipo 2, por sus siglas en inglés (SARS- CoV-2), identificado en la ciudad de Wuhan, en China (Trilla, 2020). En México, el brote llegó poco después, ya que el primer caso se registró el 27 de febrero de 2020, y para el 30 de abril, el número de pacientes aumentó exponencialmente, alcanzando un total de 19,224 casos confirmados y 1,859 (9.67%) fallecidos (Suárez et al., 2020).
Con la aparición del nuevo coronavirus, y ante la falta de tratamientos y/o vacunas (en el año 2020) para prevenirlo, se iniciaron estudios administrando diversos medicamentos para el tratamiento de enfermedades virales, respiratoria e inflamatorias, como Atazanavir, Cloroquina, Favipiravir, Hidroxicloroquina (HCQ), Lopinavir, Remdesivir, Ribavirina, Tocilizumab, entre otros, tales como medicamentos monclonales los cuales no son considerados en este estudio. Sin embargo, existen pacientes con comorbilidades que pueden verse afectados por la coadministración de estos medicamentos. Es por ello que existe la necesidad de realizar un estudio para abordar este problema, con el objetivo de elegir el mejor medicamento para cada paciente y realizar una prescripción personalizada. A continuación, se presentan un acercamiento a los medicamentos mencionados anteriormente y su uso para combatir el virus causado por el SARS-CoV-2.
Entre los fármacos que se estudiaron como posibles tratamientos se encuentra el atazanavir, este es un análogo del sustrato de la cadena peptídica aprobado para tratar el Virus de Inmunodeficiencia Humana (VIH), y que tiene el potencial de prevenir la pro-forma de proteínas del SARS-CoV-2 que se escinden en la forma de trabajo y en experimentos in-vitro recientes (Yu et al., 2020). Este medicamento inhibió la replicación del SAR-CoV-2 y las citocinas proinflamatorias (Bo Ram et al., 2020).
En el caso de la cloroquina, un ensayo de tiempo de adición realizado por Wang et al (2020), demostró su alta efectividad en la reducción de la réplica viral, con una concentración efectiva (CE) 90 de 6.90 µM, que se puede lograr fácilmente con la dosificación estándar debido a su penetración favorable en los tejidos e incluso en los pulmones. Cabe destacar que este fármaco es seguro, económico y efectivo en infecciones virales en estudios preclínicos (Cortegiani et al., 2020).
Otro fármaco es el antiviral favipiravir, que es administrado para tratar la gripe y el ébola. Favipiravir demostró ser prometedor en los primeros ensayos para el tratamiento del SARS-CoV 2. Además, su perfil de seguridad favorable con respecto a los eventos adversos totales y graves (Pilkington et al., 2020).
En cuanto a la HCQ, el trabajo de Manic et al. (2014) menciona que este fármaco tiene acciones de farmacocinética y metabolismo similares a los de la cloroquina como agente antipalúdico y autoinmune, al secuestrar protones en los lisosomas, la HCQ aumenta el pH intracelular en las células presentadoras de antígeno, lo cual es necesario para la fusión virus/ célula (Schrezenmeier y Dörner, ٢٠٢٠). También se demostró que suprime la replicación del SARS-CoV-2 al interferir con la glucosilación de su receptor celular ACE2 (Yu et al., 2020).
Un estudio realizado por Sallard, Lescure, Yazdanpanah, Mentre y Peiffer-Smadja (2020) muestra que el interferón Beta 1 puede representar un tratamiento seguro para tratar el SARS-CoV-2 en las primeras etapas de la infección.
Otro ejemplo es el lopinavir (LPV/r), un agente antirretroviral, impulsado por el ritonavir, que se usa ampliamente para tratar el VIH. Se ha informado experiencias del uso de LPV/r para tratar el SARS-CoV-2 con resultados positivos (Cheng, et al., 2020).
El remdesivir, como menciona el trabajo realizado por Singh et al. (2020), es un fármaco antiviral de amplio espectro que ha demostrado inhibir el SARS-CoV-2, in vitro e in vivo. Este fármaco se ha probado para un uso compasivo en casos graves de SARS-CoV-2, y ha mostrado resultados mixtos, con un efecto secundario mínimo. Este fármaco recibió la autorización de uso de emergencia para pacientes hospitalizados por SARS-CoV-2 en estado grave en adultos y niños.
Ribavirina es un fármaco con amplia disponibilidad y bajo costo, lo que respalda el potencial para que impacte de manera significativa en el tratamiento de las infecciones por el SARS-CoV-2. La eficacia de ésta fue evaluada desde el año 2003 durante el primer brote de SARS y en el 2013 en el brote de Síndrome Respiratorio de Medio Oriente (MERS), lo que llevó a la evaluación resumida de su utilidad en el tratamiento de pacientes con SARS-CoV-2 (S. Khalili et al., 2020).
El estudio realizado por Capra (2020), apoya la eficacia de una dosis baja única de tocilizumab en casos de neumonía causada por SARS-CoV-2 grave, ya que mostró una tasas de supervivencia significativamente más altas en pacientes tratados contra pacientes que no han tenido acceso a la inhibición soluble del receptor de IL-6. El efecto del tratamiento se realizó de manera independiente a las condiciones clínicas basales como la edad, comorbilidades como diabetes, hipertensión, niveles de PCR o enfermedades del corazón. Tomando en cuenta a los pacientes cuyo resultado se conoce, el número de pacientes completamente recuperados fue más alto en el grupo de pacientes que recibieron tocilizumab (92%), en comparación con el grupo de pacientes que recibieron solo atención estándar (42.1%). Además, para pacientes aún hospitalizados, se describió un curso clínico más favorable en pacientes que recibieron tocilizumab en términos de soporte respiratorio y saturación arterial de oxígeno (SpO2).
Para este estudio de las interacciones de medicamentos que se han propuesto como posibles tratamientos para combatir el SARS-CoV-2, se han utilizado técnicas de inteligencia artificial (IA), que incluyen conceptos transversales relacionados con la lógica y el aprendizaje, tratando de diseñar herramientas informáticas que simulen procesos de inteligencia humana que incluyen el aprendizaje, razonamiento y autocorrección. (Quesada-Varela et al., 2020).
La IA constituye uno de los campos interdisciplinarios y transfronterizos donde convergen diferentes ciencias. Muchas de las esferas que emplean estas técnicas, incluidas las ciencias médicas, consideran esencial a la IA entre sus líneas estratégicas de investigación, debiendo a ella los resultados obtenidos en el proceso de cierto tipo de problemas médicos, como el diagnóstico y el tratamiento de diversas enfermedades (Gallardo y Ávila, 2008)
La ventaja principal del uso de redes neuronales (RN) es su capacidad de incorporar efectos no-lineales e interacciones entre las variables del modelo sin necesidad de incluirlas a priori. Como mayores desventajas, las RN proporcionan un modelo donde es difícil la interpretación de los parámetros, y que necesita de un cierto empirismo en su proceso de construcción y entrenamiento. Sin embargo, son útiles para el cálculo de la probabilidad de un resultado en función de un conjunto de variables predictoras consiguiendo buenos resultados (Javier Trujillano, 2004)
Recientemente se han utilizado una gran cantidad de recursos para poder obtener una detección temprana del paciente infectado. Imran et al (2020) construyeron un motor de IA centrado en el mediador triple para el diagnóstico basado en la tos de COVID-19, denominado AI4COVID-19. Los resultados obtenidos mostraron que AI4COVID-19 puede ser capaz de diagnosticar SARS-CoV-2 con una probabilidad de diagnóstico erróneo insignificante gracias a su arquitectura de prevención de riesgos.
Otro caso en el que se involucra a la IA es la reutilización de fármacos, es decir, utilizar medicamentos ya existentes para poder tratar el SARS-CoV-2. Reyna (2020) demostró que existe una gran similitud entre el SARS-CoV y el SARS-CoV-2. Sree et al. (2019) argumentan que se pueden crear modelos de IA para predecir las estructuras farmacológicas que podrían tratar el SARS-CoV-2. La IA y el aprendizaje profundo pueden respaldar este procedimiento al reconocer rápidamente los medicamentos que son adecuados contra el SARS-CoV-2, y así poder superar barreras entre tantos medicamentos reutilizados, pruebas de laboratorio/clínicas y la autorización final de medicamentos (Mohanty et al., 2020).
Otros enfoques se han utilizado para evaluar la coadministración de medicamentos a pacientes con SARS-CoV-2. Awortwe y Cascorbi (2020) realizan un meta-análisis para determinar las comorbilidades observadas en el curso de la enfermedad por SARS-CoV-2 asociadas con un mayor riesgo de empeoramiento de los resultados clínicos de 24 estudios publicados. En su estudio encontraron interacciones a nivel farmacocinético entre los agentes antivirales Atazanavir y Lopinavir/Ritonavir y algunos medicamentos utilizados en el tratamiento de enfermedades cardiovasculares, como antiarrítmicos y anticoagulantes, que pueden afectar el resultado clínico.
Con lo anterior, se puede decir que la IA es una herramienta que puede aplicarse exitosamente en áreas como la medicina, y que tiene el potencial de evaluar el riesgo de interacción entre fármacos ya que lo puede hacer de una manera rápida y eficaz, lo que permite la respuesta rápida del personal médico.
En la Tabla 1 se muestran los trabajos relacionados con el presente estudio, con base a esto, podemos observar que se han realizado proyectos que implican la aplicación de técnicas de inteligencia artificial y el diagnóstico médico; sin embargo, ninguno de estos toma en cuenta la coadministración de fármacos y el uso de redes neuronales para asistir a los médicos en la correcta administración del tratamiento.
Tabla 1
Estado del arte
|
Titulo |
Autor (es) |
Journal |
Metodología y técnicas |
Objetivo del estudio |
|
Inteligencia Artificial para Asistir el Diagnóstico Clínico en Medicina |
Lugo-Reyes, et al., 2014 |
Revista Alergia México |
Minería de datos, redes neuronales, entre otros. |
Recopilación de fundamentos y aplicaciones de técnicas de inteligencia artificial para la ayuda en el diagnóstico clínico |
|
Aplicación de las Redes Neuronales en Medicina |
Vega, 2016 |
Revista de ciencias de la salud y medicina, 4, 76-81 |
Redes neuronales |
Predecir la presencia de nodos linfáticos cancerígenos mediante la aplicación de redes neuronales del tipo multicapa, alcanzando un 100% en los datos de predicción |
|
Drug Interactions—Principles, Examples and Clinical Consequences |
Cascorbi, 2012 |
Dtsch Arztebl Int, 109(33–34), 546–56 |
Revisión selectiva de la literatura |
Estudiar el efecto de las interacciones farmacológicas y sus consecuencias |
|
Design of Fuzzy Expert Systems and Its Applications in Some Medical |
Allahverdi, 2014 |
Advanced Technology & Science, 2(1), 1-8 |
Lógica difusa |
Aplicación de la lógica difusa para el diagnóstico, tratamiento, predicción de riesgo etc, de diversas enfermedades |
|
Sistema De Control Difuso Para Unidades De Cuidado Intensivo |
J. Steven,2013 |
Universidad católica de Colombia |
Lógica difusa |
Se describe un método de entrenamiento difuso para generar un sistema de control difuso que permita la administración de medicamentos esenciales para la estabilidad de los signos vitales de un paciente en una unidad de cuidado intensivo |
Nota. Creación propia
1. Método
Cuando un paciente ingresa a un hospital con los síntomas típicos descritos por los especialistas cuando se trata de una infección por el SARS-CoV-2, se debe realizar una prueba para confirmar que se trata de esta enfermedad y aplicar el tratamiento adecuado, sin embargo, no siempre se cuenta con el tiempo suficiente para crear un historial médico completo, e incluso no se cuenta con el personal adecuado, por lo que al no ser especialistas en el tema no cuentan con la información completa del desempeño de cada fármaco, así como las interacciones que pueden darse con las comorbilidades presentadas por el paciente, de esta forma deben decidir de acuerdo a su experiencia, lo cual podría llevar al paciente a presentar complicaciones.
La metodología propuesta se basa en una secuencia de actividades que contribuyen a la construcción de una red neuronal artificial y está constituida en cuatro etapas.
En la etapa uno, se definen las variables de entrada del modelo, las cuales corresponden a “categorías de los medicamentos”. La variable de salida es “recomendación al coadministrar medicamentos para comorbilidades y los utilizados para el tratamiento de pacientes diagnosticados con SARS-CoV-2”. Iniciando con el proceso de construcción de la red neuronal artificial, en la etapa dos se realiza el entrenamiento (training) de la red. En la etapa tres se realiza la validación del modelo. En la etapa cuatro se realiza un análisis de sensibilidad para determinar cómo los valores de las variables independientes afectan a la variable dependiente. Para ello, se obtienen predicciones de coadministrar un determinado medicamento con otro, asumiendo que uno de ellos es para tratar la COVID-19 y el otro para tratar alguna otra enfermedad preexistente.
La red neuronal artificial se construyó utilizando el software NeuralTools®, donde el tipo de red es PNN (Redes neuronales probabilísticas) /GRNN (Red neuronal de regresión general). Las redes GRNN se usan para la aproximación de predicciones y funciones numéricas, mientras que las redes PNN se usan para predicciones de categorías y clasificación. Se utilizó este tipo de red neuronal artificial debido a la naturaleza de las variables y al objetivo del problema: ya que las variables de entrada son del tipo categóricas; y el objetivo es obtener predicciones categóricas de la variable de salida. Ambos tipos de redes neuronales fueron presentadas por Donald Specht en sus publicaciones “Probabilistic Neural Networks” (Specht, 1990) y “A General Regression Neural Network” (Specht, 1991).
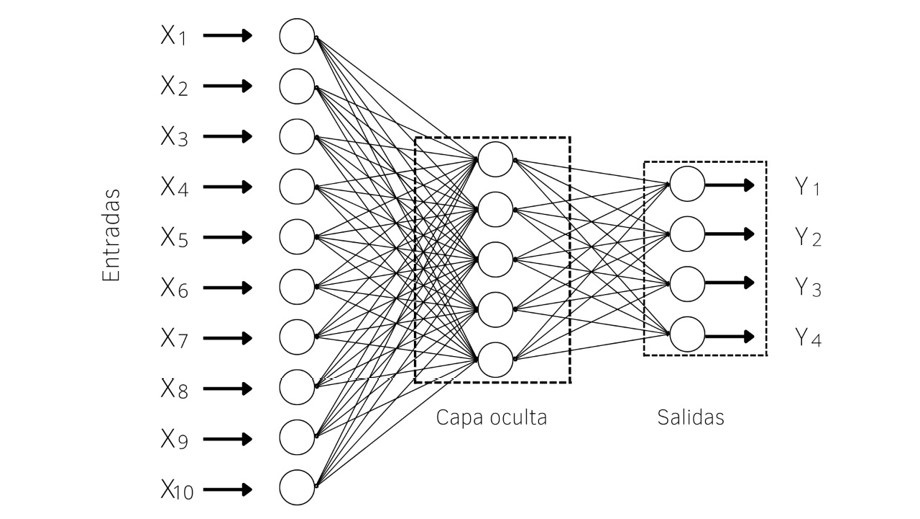
Para la etapa de entrenamiento se utiliza una base de datos de la forma ($ \bar{X}, y$), donde cada $\bar{X}=\left\{ x_1,..., x_d\right\}$ contiene d variables de entrada y $y\: \in \left\{y_1,...,y_k \right\}$. La capa de entrada contiene d nodos que transmiten d variables de entrada con bordes de pesos $\bar{W}=\left\{ w_1,...,w_d\right\}$ a la capa oculta, la cual es tiene cinco neuronas con función de activación ReLu definida en la ecuación (1).
|
$$ \phi(v)=max\left\{ v,0\right\}(Rectified\: Linear \: Unit \left [ ReLU\right ]) $$ |
Esta capa es conectada a la capa de salida, para la cual se utiliza la función Softmax. En donde, dada una instancia $x$, la función de regresión Softmax computa el puntaje $s_k(x)$ para cada clase $k$, posteriormente estima la probabilidad de que dicha instancia pertenezca a cada clase por medio de la función softmax en la ecuación (2)
|
$$ \hat{p}_k=\frac{\mathrm{exp}(s_k(x))}{\sum_{j=1}^{k}\mathrm{exp}(s_j(x))} $$ |
En donde $k$ representa el número de clases, $s_k(x)$ es el vector conteniendo los puntajes de cada clase para la instancia $x$, y $\hat{p}_k$ es la probabilidad estimada de que la instancia $x$ pertenezca a la clase $k$, de acuerdo al puntaje dado en cada clase para la respectiva instancia.
La figura 1 muestra la arquitectura de la red neuronal utilizada en este estudio, en donde se tienen diez neuronas en la capa de entrada, cinco neuronas en la capa oculta, y cuatro en la capa de salida. Estas corresponden a las diez variables de entrada del modelo, y las cuatro clases de salida. Detalles de los parámetros utilizados se presentan en la sección 2.2.
Figura 1
Metodología propuesta para el desarrollo de la red neuronal artificial.
1.1. Selección de variables
Como variables de entrada se seleccionaron los medicamentos aplicados específicamente para el tratamiento de SARS-CoV-2, a cada uno se le asignó una abreviatura para su identificación (Tabla 2).
Tabla 2
Tratamientos específicos de SARS-CoV-2.
|
Abreviatura |
Medicamento |
|
ATV |
Atazanavir |
|
CLQ |
Cloroquina |
|
FAVI |
Favipiravir |
|
HCLQ |
Hidroxicloroquina |
|
INF-B |
Interferón beta |
|
LPV/r |
Lopinavir/ritonavir |
|
RDV |
Remdesivir |
|
RBV |
Ribavirina |
|
TCZ |
Tocilizumab |
Nota: Elaboración propia.
Cada uno de estos tratamientos tienen diferentes respuestas de acuerdo a su interacción con otros fármacos para el tratamiento de otros padecimientos, síntomas o enfermedades crónicas. Es por ello que también se seleccionaron medicamentos de diez categorías diferentes, mostradas en la Tabla 3.
Tabla 3
Categorías de medicamentos para evaluar las interacciones con tratamientos de SARS-CoV-2.
|
Anestésicos y relajantes musculares |
Anitibióticos |
Antidiabéticos |
Antivirales-VHC ADD * |
Agentes gastrointestinales |
Hipertensión-Antagonistas de la angiotensina |
Hipertención- Hipertensión pulmonar |
Antiarrítmicos |
Hipertensión- Inhibidores de la ECA ** |
Inmunosupresores |
|
Alcuronio |
Ampicilina |
Acarbosa |
Elbasvir/Grazoprevir |
Alosetrón |
Candesartán |
Ambrisentán |
Amiodarona |
Benazepril |
Adalimumab |
|
Bupivacaína |
Azitromicina |
Canagliflozina |
Glecaprevir/Pibrentasvir |
Antácidos |
Eprosartán |
Bosentán |
Bepridil |
Captopril |
Globulina anitimocítica |
|
Cisatracurio |
Bedaquilina |
Dapagliflozin |
Ledipasvir/Sofosbuvir |
Bisacodilo |
Irbesartán |
Epoprostenol |
Disopiramida |
Cilazapril |
Azatioprina |
|
Desflurano |
Ciprofloxacina |
Dulaglutida |
Ombitasvir/Paritaprevir/r |
Cimetidina |
Losartán |
Lloprost |
Dofetilida |
Enalapril |
Basiliximab |
|
Dexmedetomidina |
Claritromicina |
Empagliflozina |
Ombitasvir/Paritaprevir/r + Dasabuvir |
Cisaprida |
Olmesartán |
Macitentan |
Flecainida |
Fosinopril |
Belatacept |
|
Enflurano |
Clindamicina |
Exenatida |
Sofosbuvir |
Esomeprazol |
Telmisartán |
Riociguat |
Lidocaína |
Lisinopril |
Ciclosporina |
|
Efedrina |
Clofazimina |
Glibenclamida |
Sofosbuvir/Velpatasvir |
Famotidina |
Valsartán |
Selexipag |
Mexiletine |
Perindopril |
Micofenolato |
|
Etidocaína |
Delamanid |
Gliclazida |
Sofosbuvir/Velpatasvir/Voxilaprevir |
Lactulosa |
Sildenafil |
Propafenona |
Quinapril |
Pirfenidona |
|
|
Halotano |
Eritromicina |
Glimepirida |
Lansoprazol |
Tadalafil |
Quinidina |
Ramipril |
Sirolimus |
||
|
Isoflurano |
Levofloxacina |
Glipizida |
Loperamida |
Treprostinil |
Trandolapril |
Tacrolimus |
|||
|
Ketamina |
Linezolid |
Insulina |
Mesalazina |
||||||
|
Minaxolona |
Metronidazol |
Linagliptina |
Omeprazol |
||||||
|
Óxido nitroso |
Moxifloxacina |
Liraglutida |
Pantoprazol |
||||||
|
Propofol |
Ofloxacina |
Metformina |
Prucalopride |
||||||
|
Rocuronio |
Pirazinamida |
Nateglinida |
Rabeprazol |
||||||
|
Sevoflurano |
Rifabutina |
Pioglitazona |
Ranitidina |
||||||
|
Sufentanilo |
Rifampicina |
Repaglinida |
Senna |
||||||
|
Suxametonio |
Rifapentina |
Rosiglitazona |
|||||||
|
Tetracaína |
Sulfadiazina |
Saxagliptina |
|||||||
|
Tiopental |
Telitromicina |
Sitagliptina |
|||||||
|
Tizanidina |
Tinidazol |
Tolbutamida |
|||||||
|
Vecuronio |
Trimetoprima |
Vildagliptina |
Nota: Creación propia.
*Antivirales-VHC-ADD; antivirales de acción directa para el tratamiento de la Hepatitis tipo C
** Inhibidores de la ECA; inhibidores la de enzima convertidora de angiotensina
A cada interacción se le asignó un valor numérico para representar el nivel de reacción al ser coadministrados, este número se les asignó de acuerdo al código de colores según Liverpool University (2020): al color rojo se le asignó el número 1 y representa los medicamentos, que por su reacción al ser mezclados, no deben ser coadministrados en lo absoluto.
Por otro lado, al color verde se le asignó el número 4, siendo este el caso en que la coadministración de fármacos no es significativa, es decir, no representa ningún riesgo. Estos valores representan las variables de salida de la red neuronal artificial construida. La Tabla 4 muestra la respuesta ante la interacción y el código asignado.
Tabla 4
Variables de respuesta
|
Código |
Respuesta ante la interacción* |
|
1 |
Estos medicamentos no deben ser coadministrados. |
|
2 |
Interacción potencial la cual puede requerir un ajuste de la dosis o una estrecha vigilancia. |
|
3 |
Es probable que la interacción potencial sea de intensidad débil. Es poco probable que se requieran acciones de monitoreo adicionales o un ajuste de dosis. |
|
4 |
No se espera ninguna interacción clínica significativa. |
Nota: Creación propia.
*Clasificación por Liverpool Drug Interactions Group, University of Liverpool, Pharmacology Research Labs (2020)
Un ejemplo de las interacciones y sus respuestas se observa en la Tabla 5, estos datos se utilizaron para el entrenamiento de la red, la cual puede interpretarse de la siguiente forma: “Si el paciente toma Amiodarona, Bepridil, Disopiramida, Dofetilida o Flecainida como antiarrítmico, entonces no se debe coadministrar Atazanavir como tratamiento para tratar el SARS-CoV-2. Por otro lado, si un paciente ingiere Mexiletina como antiarrítmico, puede ingerir Atazanavir para tratar el SARS-CoV-2, y esto no tendrá una interacción negativa”.
Tabla 5
Respuesta ante la coadministración de medicamentos
|
Medicamento |
Categoría / Antiarrítmicos |
Resultado |
|
ATV |
Amiodarona |
1 |
|
ATV |
Bepridil |
1 |
|
ATV |
Disopiramida |
1 |
|
ATV |
Dofetilida |
1 |
|
ATV |
Flecainida |
1 |
|
ATV |
Lidocaína |
2 |
|
ATV |
Mexiletina |
4 |
|
ATV |
Propafenona |
2 |
|
ATV |
Quinidina |
1 |
Nota: Creación propia.
1.2. Entrenamiento
Con base en el procedimiento anterior se obtienen 1134 interacciones diferentes, las cuales se utilizaron para llevar a cabo el entrenamiento de la red neuronal artificial. La red neuronal construida consta de 10 neuronas para la capa de entrada, 20 neuronas para la capa oculta, y una neurona en la capa de salida. Cada neurona en la capa de entrada corresponde a las categorías de los medicamentos de la Tabla 2, mientras que la capa de salida corresponde al valor de la predicción de acuerdo a la Tabla 3. El modelo fue construido utilizando el software NeuralTools®.
NeuralTools® es un software con licencia propiedad de Palisade Corporation®, el cual, a su vez, forma parte del conjunto de programas del software DecisionTools®, que funciona como un complemento de Microsoft Excel, que permite la configuración de redes neuronales, de acuerdo a los objetivos buscados, de una forma práctica para el usuario, con resultados gráficos y numéricos que permiten la mejor interpretación. Para propósitos de este estudio, los parámetros de entrenamiento se configuraron de la siguiente forma: épocas = 1000, meta = cero, tasa de aprendizaje = 0.001, función de activación sigmoide y la función de pérdida definida en la ecuación (3) para evaluar el error del modelo.
Los resultados del entrenamiento se muestran en la Tabla 6, en la que se observa que se obtuvo un 0% de malas predicciones usando un porcentaje de tolerancia del 30% y que el error medio absoluto es cero, al igual que la desviación estándar del error absoluto para los 1134 casos evaluados. Estos resultados demuestran un entrenamiento eficiente de la red neuronal artificial.
Tabla 6
Resultados de la etapa de entrenamiento de la red neuronal artificial; Neural Tools, Excel
|
Entrenamiento |
|
|
Número de Casos |
1134 |
|
Tiempo de Entrenamiento |
00:12:02 |
|
Número de Ensayos |
0 |
|
Motivo de Termino |
Detención automática |
|
% Malas Predicciones (30%) |
0.0000% |
|
Error Cuadrático Medio |
0.0000000000 |
|
Error Medio Absoluto |
0.0000000000 |
|
Desviación Estándar del Error Absoluto |
0.0000000000 |
1.3. Validación
La validación se llevó a cabo igualmente mediante la herramienta NeuralTools® de Excel, donde se utilizaron los 99 casos restantes, obteniendo como resultado de las pruebas que se tiene alrededor del 9.0% de malas predicciones con un porcentaje de tolerancia del 30%, con un error medio absoluto (EMA) de 0.15 y una desviación estándar (DE) de 0.42 para los 99 casos. En este tipo de validaciones se tiene por objetivo obtener un valor de EMA cercano a cero, lo que nos diría que la diferencia entre los valores observados y los encontrados con la red neuronal son muy parecidos, lo que a su vez indica que los resultados son representativos del sistema original, en este caso específico el valor encontrado indica que las predicciones son representativas. En el caso de la DE indica que el valor de dispersión de los datos es del 42%, lo cual, por propósitos del estudio y disponibilidad de datos se considera aceptable.
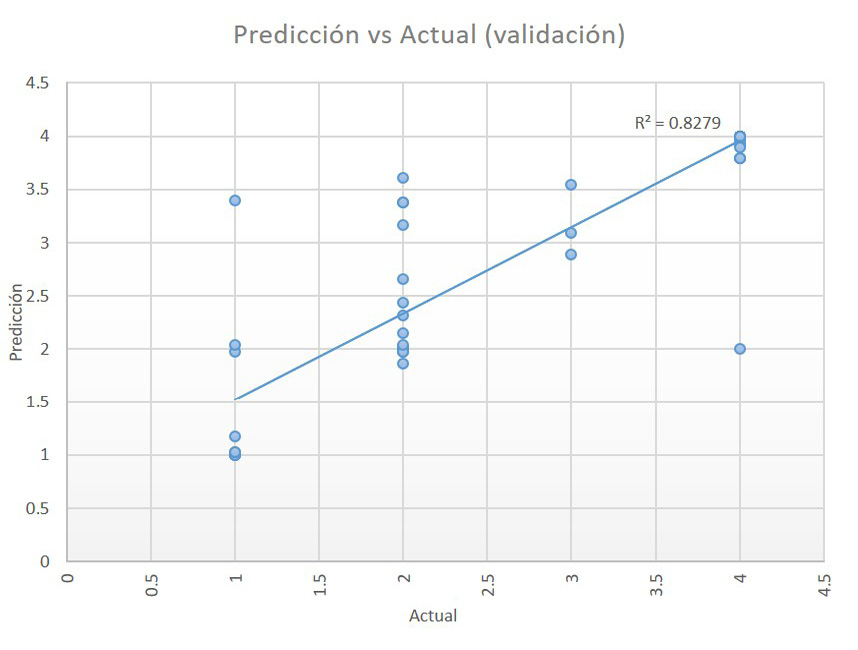
En la Figura 2 se muestra la gráfica de los resultados obtenidos durante la validación, la correlación de las predicciones contra los valores reales, en la que se observa que se obtuvo un valor del 0.8279 para el coeficiente de determinación, para dicho coeficiente, cuyos valores oscilan entre 0 y 1, se considera que un valor cercano a uno representa un mayor ajuste del modelo, es decir mayor fiabilidad en las predicciones; de forma inversa cuanto más cercano a cero, el modelo será menos fiable. El valor obtenido para este modelo demuestra que los resultados obtenidos por la red neuronal artificial son confiables y representativos del sistema original.
Figura 2
Gráfica de resultados de la validación de la red neuronal artificial
1.4. Predicciones
Para obtener las predicciones se debe colocar primeramente el medicamento especializado que se quiere administrar para tratar la COVID-19 y en las celdas siguientes colocar los medicamentos que el paciente necesita de acuerdo al padecimiento categorizado en la Tabla 2. Un ejemplo de esto se muestra en la Tabla 7, en la que se pueden observar tres escenarios:
Si se quiere administrar Atazanavir (tratamiento para SARS-CoV-2), Enflurano (Anestésicos & Relajantes Musculares) y Azatioprina (Inmunosupresor), el resultado de la interacción de estos medicamentos es 4, es decir, no hay riesgo significativo al coadministrar estos medicamentos.
Si se pretende usar Remdesivir (tratamiento para SARS-CoV-2) y Metformina (Antidiabéticos) el resultado de esta interacción es que no existe riesgo significativo al coadministrar estos fármacos, ya que el resultado de la variable de salida es 4.
Si se quiere es administrar Cloroquina (tratamiento para SARS-CoV-2), Metformina (Antidiabéticos) y Azatioprina (Inmunosupresor) se obtiene como resultado 2, lo que indica una interacción potencial que requiere un reajuste en las dosis o monitoreo constante.
Tabla 7
Predicciones usando redes neuronales artificiales
|
Tratamiento COVID-19 |
Anestésicos y relajantes musculares |
Antibacteriales |
Antidiabéticos |
Antivirales-VHC ADD |
Agentes gastrointestinales |
Hipertensión-Antagonistas de la angiotensina |
Hipertención- Hipertensión pulmonar |
Antiarrítmicos |
Hipertensión- Inhibidores de la ECA |
Inmunosupresores |
Resultado |
|
ATV |
Enflurano |
- |
- |
- |
- |
- |
- |
- |
- |
Azatioprina |
4 |
|
RDV |
- |
- |
Metformina |
- |
- |
- |
- |
- |
- |
- |
4 |
|
CLQ |
- |
- |
Metformina |
- |
- |
- |
- |
- |
- |
Azatioprina |
2 |
Nota: Creación propia
2. Resultados
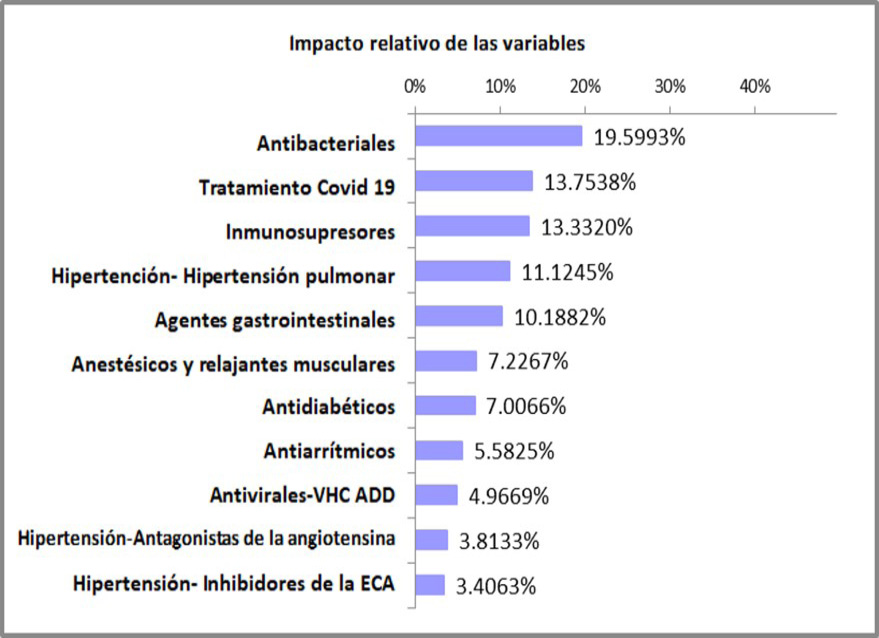
Como primer resultado se obtuvo el porcentaje de impacto de cada variable de entrada, la cual se muestra en la Figura 3. Como se puede observar, el uso de antibacteriales es la variable de mayor impacto con un 19.59%, seguida por los medicamentos o tratamientos específicos para SARS-CoV-2con un 13.75%, en tercer lugar, el uso de inmunosupresores con un 13.33%. Estos porcentajes indican el cuidado especial que el especialista debe tener al coadministrar los medicamentos de cada categoría, en conjunto con la administración de medicamentos para tratar el SARS-CoV-2.
Figura 3
Impacto relativo de la interacción entre medicamentos
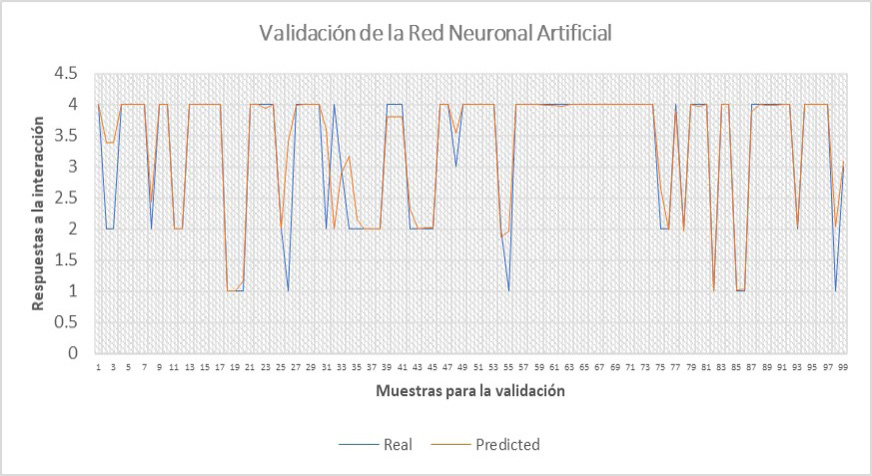
Los resultados de las pruebas, con 99 casos nuevos, muestran un coeficiente de determinación ($R^_2$) de 82.79%, logrando buena confianza en las predicciones y asegurando que sean exitosas, como se describió anteriormente. Los resultados detallados se muestran en el Anexo A. La Figura 4 muestra la validación de la red neuronal artificial, en donde la línea azul representa los datos obtenidos de la base de datos, mientras que la roja muestra los obtenidos o predichos por la red neuronal artificial, en este caso, gráficamente se busca que ambas líneas presenten un comportamiento similar, lo que indica que los datos obtenidos son representativos del modelo real, lo que a su vez, demuestra que es posible usar la red neuronal artificial como herramienta ante la predicción de la respuesta en pacientes con comorbilidades tratados con los diferentes fármacos presentados anteriormente.
Figura 4
Validación de la predicción de la red neuronal artificial para 99 casos
A partir de los resultados de la red neuronal artificial se pueden obtener los resultados de la interacción de la administración de medicamentos para tratar el SARS-CoV-2 y la coadministración de otros medicamentos para tratar comorbilidades o complicaciones en el paciente. Es por ello que, este trabajo puede ser utilizado como un sistema de apoyo a las decisiones clínicas para ayudar a elegir el mejor medicamento para el tratamiento de SARS-CoV-2, cuando simultáneamente se debe coadministrar algún otro y viceversa.
3. Discusión
La capacidad de respuesta del personal médico ante una contingencia sanitaria, como lo es la pandemia causada por el SARS-CoV-2, es crucial. Dada la saturación de los hospitales y el riesgo de contagio del personal, es importante contar con herramientas que permitan tomar las mejores decisiones en el menor tiempo posible, tomando en cuenta los síntomas de los pacientes, así como sus respectivas comorbilidades. Debido a que no existe un modelo que considere el uso de las mismas variables de entrada y salida, así como el mismo método de IA, es aventurado realizar comparaciones entre este y los desarrollados anteriormente, aun así, se puede observar la marcada tendencia en la aplicación de nuevas técnicas que brinden herramientas a los especialistas con el fin de mejorar la atención brindada a los pacientes. Este modelo es flexible y eficiente, y permite al personal médico tomar decisiones acertadas sin la necesidad de ser especialistas en la interacción de la enfermedad infecciona del SARS-CoV-2con las comorbilidades de los pacientes.
Para la construcción de la red neuronal artificial se utilizó una base de datos de interacciones farmacológicas, donde se presentan nueve tratamientos indicados en el tratamiento de esta enfermedad y las respuestas que podrían presentar en combinación con 10 diversos grupos de medicamentos utilizados para el tratamiento de otros padecimientos. Se estableció una codificación para los diversos niveles de respuesta, para ayudar a identificar de forma más eficiente el riesgo de coadministración de estos. Aunque la base de datos contaba con otras clasificaciones, se seleccionaron estas 10 debido a que cumplen con las características necesarias para alcanzar un entrenamiento adecuado de la red neuronal artificial.
Tomando en cuenta lo anterior, se diseñó una red neuronal artificial capaz de proporcionar soporte a la decisión al personal médico encargado de prescribir el tratamiento de pacientes con SARS-CoV-2, evitando con esto posibles complicaciones. Además, esta red se desarrolló de tal manera que el usuario pueda operarla con facilidad, y aunque implica un alto nivel de conocimiento de los medicamentos, las entradas y salidas se muestran de manera simplificada e interpretable.
La cantidad de escenarios que pueden presentarse durante el desarrollo de esta nueva enfermedad es muy extensa y compleja. Por tal motivo, puede ser muy complejo enumerar las diversas interacciones entre los pacientes afectados por la contingencia sanitaria y los múltiples tratamientos disponibles. A todo esto se debe agregar la formación y experiencia del personal médico y profesionales de la salud, los cuales pueden tener diferentes opiniones y tender a prescribir determinados medicamentos a sus pacientes considerando su experiencia. Por tal motivo, el uso de herramientas de inteligencia artificial puede contribuir a minimizar el riesgo de cometer errores por omisión por parte del personal médico; además de que dichas técnicas tienen la capacidad de procesar y extraer información de grandes cantidades de datos. Cabe destacar que el uso de estas técnicas, como el uso de redes neuronales artificiales en este trabajo, no pretenden sustituir al personal médico experto, sino que son diseñadas como una herramienta de apoyo a la decisión clínica.
Actualmente se han desarrollado diferentes trabajos utilizando redes neuronales artificiales y aprendizaje profundo para el diagnóstico de infecciones nosocomiales e infecciones respiratorias agudas, tales como los trabajos de Hassan et al. (2020), en el que los autores utilizan redes neuronales recurrentes para la detección del COVID-19. Por otro lado, Narin et al. (2021) desarrollaron un sistema para la detección automática de COVID-19 utilizando redes neuronales artificiales e imágenes de rayos-x. Estos trabajos se centran en la detección de una enfermedad. Por otro lado, la investigación desarrollada en este artículo se centra en la evaluación de la interacción de medicamentos utilizados para tratar el COVID-19 (en el año 2020 principalmente) y otro grupo de medicamentos para tratar enfermedades pre-existentes. Esto permite al personal médico tener una herramienta de apoyo a la decisión para realizar una prescripción más personalizada para los pacientes, y con ello reducir el riesgo de un efecto negativo al tratar al COVID-19, al mismo tiempo que se combaten otras enfermedades pre-existentes.
4. Conclusiones
En la actualidad, a pesar de los esfuerzos del personal médico y de salud, y de las tecnologías, se ha denotado que existe cierta incapacidad para actuar de manera
adecuada ante una emergencia sanitaria sin precedente, como se vio desde la antigüedad, las pandemias han cobrado la vida de millones de personas en el mundo, y en este caso no ha sido la excepción; no obstante, la lucha para combatir las enfermedades que aquejan a la población no cesa y se busca emplear todos los métodos y técnicas disponibles para este propósito, y la inteligencia artificial no queda a un lado, ya que, por su flexibilidad, es capaz de adaptarse a casi todos las áreas, como en este caso, la medicina.
El objetivo principal de este trabajo es proporcionar un sistema de apoyo a la decisión para
evaluar la coadministración de medicamentos a pacientes confirmados con SARS-CoV-2. La metodología propuesta ayuda a evaluar los distintos medicamentos y su efecto en la
coadministración con tratamientos específicos para tratar el SARS-CoV-2 dando una respuesta rápida y eficiente, tal como se demostró al realizar predicciones con la red neuronal artificial planteada.
La aplicación de dicha red neuronal artificial concluye en la mejor determinación de tratamientos a administrar en pacientes en diversas etapas de SARS-CoV-2, disminuyendo con esto el riesgo de consecuencias nocivas e incluso irreversibles en la salud del paciente, ambicionando la reducción en los casos de decesos por una incorrecta coadministración de fármacos.
De una forma secundaria, la implementación del sistema, podría reducir costos de hospitalización, por insumos, por el personal médico y el uso de las instalaciones, dado que una medicación errónea produce complicaciones que, en el mejor de los casos, aumenta el tiempo del paciente en el hospital, e incluso la carga de trabajo para los doctores y enfermeras, saturando así los hospitales, ya que en este tipo de situaciones, las decisiones que podrían parecer más insignificantes, resultan ser las de mayor repercusión.
Con base en el análisis de resultados presentado en la sección 4, se puede decir que los resultados obtenidos al evaluar el modelo fueron satisfactorios, siendo este 82.79%. Sin embargo, se podrían obtener mejoras considerables al considerar otros parámetros y arquitecturas del modelo. Por ejemplo, se podría incrementar la precisión del modelo al considerar y evaluar diferentes arquitecturas, tales como agregar más capas ocultas y el número de neuronas en cada capa. Sin embargo, esto conlleva que el entrenamiento de la red sería más costoso en términos de complejidad computacional. No obstante, se podría explorar métodos de optimización para encontrar la arquitectura optima de la red neuronal propuesta, ya sea realizando una búsqueda de arquitectura en un espacio discreto, utilizando, por ejemplo, el enfoque de Liu et al. (2018); o en un espacio continuo, utilizando, por ejemplo, el enfoque descrito en el trabajo de Luo et al. (2018).
Fuentes de financiamiento
El presente trabajo fue financiado por el Consejo Nacional de Ciencia y Tecnología (CONACyT) a través de becas de Maestría del PNPC.
Declaratoria de disponibilidad de datos
Los datos para esta investigación son de acceso abierto y están disponibles en https://www.covid19-druginteractions.org/prescribing-resources
Referencias
Awortwe, C. y Cascorbi, I. (2020). Meta-analysis on outcome-worsening comorbidities of COVID-19 and related potential drug-drug interactions. Pharmacological Research, 161. https://doi.org/10.1016/j.phrs.2020.105250
Beck, B. R.; Shin, B.; Choi, Y.; Park, S. y Kang, K. (2020). Predicting commercially available antiviral drugs that may act on the novel coronavirus (2019-nCoV), Wuhan, China through a drug-target interaction deep learning model. bioRxiv, 18, 784-790. https://doi.org/10.1101/2020.01.31.929547
Aggarwal, C. (2018). Neural Networks and Deep Learning. Springer.
Capra, R., De Rossi, N., Mattioli, F., Romanelli, G., Scarpazza, C., Pia Sormani, M., y Cossi, S. (2020). Impact of low dose tocilizumab on mortality rate in patients with COVID-19. European Journal of Internal Medicine, 76, 31-35. https://doi.org/10.1016/j.ejim.2020.05.009
Cheng, C.-Y., Lee, Y.-L., Chen, C.-P., Lin, Y.-C., Liu, C.-E., Liao, C.-H., y Cheng, S.-H. (2020). Lopinavir/ritonavir did not shorten the duration of SARS CoV-2 shedding in patients with mild pneumonia in Taiwan. Journal of Microbiology, Immunology and Infection, 53, 488-492. https://doi.org/10.1016/j.jmii.2020.03.032
Cortegiani, A., Ingoglia, G., Ippolito, M., Giarratano, A. y Einav, S. (2020). A systematic review on the efficacy and safety of chloroquine for the treatment of COVID-19. Journal of Critical Care, 57, 279-283. https://doi.org/10.1016/J.JCRC.2020.03.005
Gallardo, M. d., y Ávila, R. Á. (2008). Artificial intelligence applied to medicine: prospects and problems. ACIMED, 17(5). Recuperado el 24 de 07 de 2020, de http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S1024-94352008000500005&lng=es&tlng=es.
GNS, H. S., GR, S., Murahari, M., y Krishnamurthy, M. (2019). An update on Drug Repurposing: Re-written saga of the drug’s fate. Biomedicine & Pharmacotherapy, 110, 700-716. https://doi.org/10.1016/j.biopha.2018.11.127
Hassan, A., Shahin, I., y Alsabek, M. B. (2020, November). COVID-19 detection system using recurrent neural networks. In 2020 International conference on communications, computing, cybersecurity, and informatics (CCCI) (pp. 1-5). IEEE.
Imran, A., Posokhova, I., Qureshi, H. N., Masood, U., Riaz, S., Ali, K., . . . Nabeel, M. (2020). AI4COVID-19: AI enabled preliminary diagnosis for COVID-19 from cough samples via an app. Informatics in Medicine Unlocked. https://doi.org/10.1016/j.imu.2020.100378
Javier Trujillano, J. M. (2004). Aproximación metodológica al uso de redes neuronales artificiales para la predicción de resultados en medicina. Medicina Clínica, 122, 59-67. https://www.elsevier.es/es-revista-medicina-clinica-2-articulo-aproximacion-metodologica-al-uso-redes-13057536
Kubat, M. (2017). Artificial neural networks. In An Introduction to Machine Learning. Springer.
Liverpool University. (2020). COVID-19 Drug Interactions. Obtenido de https://www.covid19-druginteractions.org/checker
Liu, C., Zoph, B., Neumann, M., Shlens, J., Hua, W., Li, L. J., ... y Murphy, K. (2018). Progressive neural architecture search. In Proceedings of the European conference on computer vision (ECCV) (pp. 19-34).
Luo, R., Tian, F., Qin, T., Chen, E., y Liu, T. Y. (2018). Neural architecture optimization. Advances in neural information processing systems, 31.
Manic, G., Obrist, F., Kroemer, G., Vitale, I., y Galluzzi, L. (2014). Chloroquine and hydroxychloroquine for cancer therapy. Molecular & cellular oncology. https://doi.org/10.4161/mco.29911
Mohanty, S., Rashid, M. H., Mridul, M., Mohanty, C., y Swayamsiddha, S. (2020). Application of Artificial Intelligence in COVID-19 drug repurposing. Diabetes & Metabolic Syndrome: Clinical Research & Reviews, (14), 1027-1031. https://doi.org/10.1016/j.dsx.2020.06.068
Narin, A., Kaya, C., y Pamuk, Z. (2021). Automatic detection of coronavirus disease (covid-19) using x-ray images and deep convolutional neural networks. Pattern Analysis and Applications, 24, 1207-1220.
Pilkington, V., Toby, P., y Andrew, H. (2020). A review of the safety of favipiravir – a potential treatment in the COVID-19 pandemic? Journal of Virus Eradication 6(2), 44-51. https://doi.org/10.1016/S2055-6640(20)30016-9
Quesada-Varela, V., Avila-Tomás, J., y Mayer-Pujadas, M. (2020). Artificial intelligence and its applications in medicine I: introductory background to AI and robotics. Atención primaria 52(10), 778-774. https://doi.org/10.1016/j.aprim.2020.04.013
Reyna, J. (2020). El SARS-CoV-2,una nueva zoonosis pandémica que amenaza al mundo. Vacunas, 21(1), 17-22. https://doi.org/10.1016/j.vacun.2020.03.001
S. Khalili, J., Zhu, H., Amanda Mak, N. S., Yan, Y., y Zhu, Y. (2020). Novel coronavirus treatment with ribavirin: Groundwork for an evaluation concerning COVID‐19. Journal of Medical Virology 92(7), 740–746. https://doi.org/10.1002/jmv.25798
Sallard, E., Lescure, F.-X., Yazdanpanah, Y., Mentre, F., y Peiffer-Smadja, N. (2020). Type 1 interferons as a potential treatment against COVID-19. Antiviral Research, 178. https://doi.org/10.1016/j.antiviral.2020.104791
Schrezenmeier, E., y Dörner, T. (٢٠٢٠). Mechanisms of action of hydroxychloroquine and chloroquine: implications for rheumatology. Nature Reviews Rheumatology, 16, 155-166. https://doi.org/10.1038/s41584-020-0372-x
Singh, A. K., Singh, A., Singh, R., y Misra, A. (2020). Remdesivir in COVID-19: A critical review of pharmacology, pre-clinical and clinical studies. Diabetes & Metabolic Syndrome: Clinical Research & Reviews, 14(4), 641-648. https://doi.org/10.1016/j.dsx.2020.05.018
Specht, D. F. (1990). Probabilistic Neural Networks. Neural Networks, 3(1), 109-118. https://doi.org/10.1016/0893-6080(90)90049-Q
Specht, D. F. (1991). A General Regression Neural Network. IEEE Transactions on Neural Networks, 2(6), 568-576.
Suárez, V., Suárez Quezada, M., Oros Ruiz, S., y Ronquillo De Jesús, E. (2020). Epidemiología de COVID-19 en México: del 27 de febrero al 30 de abril de 2020. Revista Clínica Española 220(8), 463-471. https://doi.org/10.1016/j.rce.2020.05.007
Trilla, A. (2020). Un mundo, una salud: la epidemia por el nuevo coronavirus COVID-19. Medicina Clínica, 154(5), 175-177. https://doi.org/10.1016/j.medcli.2020.02.002
Wang, M., Cao, R., Zhang, L., Yang, X., Liu, J., y Xu, M. (2020). Remdesivir and chloroquine effectively inhibit the recently. Cell Research, 30, 269-271. https://doi.org/10.1038/S41422-020-0282-0
Yu, W.-L., Toh, H., Liao, C.-T., y Chang, W.-T. (2020). A Double-Edged Sword—Cardiovascular Concerns of Potential Anti-COVID-19 Drugs. Cardiovascular Drugs and Therapy, 35, 205-214. https://doi.org/10.1007/S10557-020-07024-7
Anexo A
Tabla A1.
Validación de la red neuronal artificial.
|
Tratamiento COVID-19 |
Anestésicos y relajantes musculares |
Antibacteriales |
Antidiabéticos |
Antivirales-VHC ADD |
Agentes gastrointestinales |
Hipertensión-Antagonistas de la angiotensina |
Hipertención- Hipertensión pulmonar |
Antiarrítmicos |
Hipertensión- Inhibidores de la ECA |
Inmunodepresores |
Resultado |
|||||||||||
|
ATV |
Alcuronium |
- |
- |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
ATV |
Etidocaine |
- |
- |
- |
- |
- |
- |
- |
- |
- |
2 |
3.38 |
||||||||||
|
ATV |
Ketamine |
- |
- |
- |
- |
- |
- |
- |
- |
- |
2 |
3.38 |
||||||||||
|
CLQ |
Nitrous oxide |
- |
- |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
FAVI |
Minaxolane |
- |
- |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
FAVI |
Thiopenal |
- |
- |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
HCLQ |
Suxamethonium |
- |
- |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
HCLQ |
Tizanidine |
- |
- |
- |
- |
- |
- |
- |
- |
- |
2 |
2.44 |
||||||||||
|
INF-B |
Bupivacaine |
- |
- |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
INF-B |
Vecuronium |
- |
- |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
LPV/r |
Dexmedetomidine |
- |
- |
- |
- |
- |
- |
- |
- |
- |
2 |
2.00 |
||||||||||
|
LPV/r |
Propofol |
- |
- |
- |
- |
- |
- |
- |
- |
- |
2 |
2.00 |
||||||||||
|
RDV |
Isuflurane |
- |
- |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
RDV |
Nitrous oxide |
- |
- |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
RDV |
Vecuronium |
- |
- |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
RBV |
Ephedrine |
- |
- |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
RBV |
Rocuronium |
- |
- |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
ATV |
- |
Rifapentine |
- |
- |
- |
- |
- |
- |
- |
- |
1 |
1.00 |
||||||||||
|
CLQ |
- |
Erythromycin |
- |
- |
- |
- |
- |
- |
- |
- |
1 |
1.00 |
||||||||||
|
CLQ |
- |
Moxifloxacin |
- |
- |
- |
- |
- |
- |
- |
- |
1 |
1.18 |
||||||||||
|
CLQ |
- |
Pyrazinamide |
- |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
FAVI |
- |
Clarithromycin |
- |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
INF-B |
- |
Rifampicim |
- |
- |
- |
- |
- |
- |
- |
- |
4 |
3.93 |
||||||||||
|
INF-B |
- |
Rifapentine |
- |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
LPV/r |
- |
Bedaquiline |
- |
- |
- |
- |
- |
- |
- |
- |
2 |
2.00 |
||||||||||
|
RDV |
- |
Rifapentine |
- |
- |
- |
- |
- |
- |
- |
- |
1 |
3.40 |
||||||||||
|
RDV |
- |
Trimethoprim |
- |
- |
- |
- |
- |
- |
- |
- |
4 |
3.99 |
||||||||||
|
RBV |
- |
Ciprofloxacin |
- |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
RBV |
- |
Clofazimine |
- |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
TCZ |
- |
Moxifloxacin |
- |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
ATV |
- |
- |
Exanatide |
- |
- |
- |
- |
- |
- |
- |
2 |
3.61 |
||||||||||
|
ATV |
- |
- |
Gliclazide |
- |
- |
- |
- |
- |
- |
- |
4 |
2.01 |
||||||||||
|
ATV |
- |
- |
Pioglitazone |
- |
- |
- |
- |
- |
- |
- |
3 |
2.89 |
||||||||||
|
CLQ |
- |
- |
Canagliflozin |
- |
- |
- |
- |
- |
- |
- |
2 |
3.17 |
||||||||||
|
CLQ |
- |
- |
Dapagliflozin |
- |
- |
- |
- |
- |
- |
- |
2 |
2.15 |
||||||||||
|
CLQ |
- |
- |
Dulaglutide |
- |
- |
- |
- |
- |
- |
- |
2 |
2.00 |
||||||||||
|
CLQ |
- |
- |
Liraglutide |
- |
- |
- |
- |
- |
- |
- |
2 |
2.00 |
||||||||||
|
CLQ |
- |
- |
Pioglitazone |
- |
- |
- |
- |
- |
- |
- |
2 |
2.00 |
||||||||||
|
FAVI |
- |
- |
Dulaglutide |
- |
- |
- |
- |
- |
- |
- |
4 |
3.79 |
||||||||||
|
FAVI |
- |
- |
Empagliflozin |
- |
- |
- |
- |
- |
- |
- |
4 |
3.79 |
||||||||||
|
FAVI |
- |
- |
Sitagliptin |
- |
- |
- |
- |
- |
- |
- |
4 |
3.79 |
||||||||||
|
HCLQ |
- |
- |
Canagliflozin |
- |
- |
- |
- |
- |
- |
- |
2 |
2.32 |
||||||||||
|
HCLQ |
- |
- |
Exanatide |
- |
- |
- |
- |
- |
- |
- |
2 |
2.00 |
||||||||||
|
HCLQ |
- |
- |
Insuline |
- |
- |
- |
- |
- |
- |
- |
2 |
2.01 |
||||||||||
|
HCLQ |
- |
- |
Tolbutamide |
- |
- |
- |
- |
- |
- |
- |
2 |
2.02 |
||||||||||
|
INF-B |
- |
- |
Gliclazide |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
INF-B |
- |
- |
Rosiglitazone |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
LPV/r |
- |
- |
Rosiglitazone |
- |
- |
- |
- |
- |
- |
- |
3 |
3.54 |
||||||||||
|
RDV |
- |
- |
Insuline |
- |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
HCLQ |
- |
- |
- |
Sofosbuvir/Velpatasvir |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
INF-B |
- |
- |
- |
Ledipasvir/Sofosbuvir |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
TCZ |
- |
- |
- |
Glecaprevir/Pibrentasvir |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
TCZ |
- |
- |
- |
Sofosbuvir |
- |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
ATV |
- |
- |
- |
- |
Antacids |
- |
- |
- |
- |
- |
2 |
1.87 |
||||||||||
|
ATV |
- |
- |
- |
- |
Senna |
- |
- |
- |
- |
- |
1 |
1.98 |
||||||||||
|
CLQ |
- |
- |
- |
- |
Senna |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
FAVI |
- |
- |
- |
- |
Famotidine |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
FAVI |
- |
- |
- |
- |
Lansoprazole |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
FAVI |
- |
- |
- |
- |
Omeprazole |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
HCLQ |
- |
- |
- |
- |
Lansoprazole |
- |
- |
- |
- |
- |
4 |
3.99 |
||||||||||
|
HCLQ |
- |
- |
- |
- |
Rabeprazole |
- |
- |
- |
- |
- |
4 |
3.99 |
||||||||||
|
HCLQ |
- |
- |
- |
- |
Ranitidine |
- |
- |
- |
- |
- |
4 |
3.97 |
||||||||||
|
INF-B |
- |
- |
- |
- |
Bisacodyl |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
RBV |
- |
- |
- |
- |
Antacids |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
RBV |
- |
- |
- |
- |
Cimetidine |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
RBV |
- |
- |
- |
- |
Senna |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
TCZ |
- |
- |
- |
- |
Lansoprazole |
- |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
FAVI |
- |
- |
- |
- |
- |
Losartan |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
FAVI |
- |
- |
- |
- |
- |
Valsartan |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
HCLQ |
- |
- |
- |
- |
- |
Losartan |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
RBV |
- |
- |
- |
- |
- |
Irbesartan |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
RBV |
- |
- |
- |
- |
- |
Losartan |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
RBV |
- |
- |
- |
- |
- |
Olmesartan |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
RBV |
- |
- |
- |
- |
- |
Telmisartan |
- |
- |
- |
- |
4 |
4.00 |
||||||||||
|
ATV |
- |
- |
- |
- |
- |
- |
Ambrisentan |
- |
- |
- |
2 |
2.66 |
||||||||||
|
HCLQ |
- |
- |
- |
- |
- |
- |
Bosentan |
- |
- |
- |
2 |
1.98 |
||||||||||
|
INF-B |
- |
- |
- |
- |
- |
- |
Bosentan |
- |
- |
- |
4 |
3.91 |
||||||||||
|
LPV/r |
- |
- |
- |
- |
- |
- |
Tadalafil |
- |
- |
- |
2 |
1.98 |
||||||||||
|
RDV |
- |
- |
- |
- |
- |
- |
Ambrisentan |
- |
- |
- |
4 |
4.00 |
||||||||||
|
RBV |
- |
- |
- |
- |
- |
- |
Bosentan |
- |
- |
- |
4 |
3.97 |
||||||||||
|
TCZ |
- |
- |
- |
- |
- |
- |
Treprostinil |
- |
- |
- |
4 |
4.00 |
||||||||||
|
CLQ |
- |
- |
- |
- |
- |
- |
- |
Disopyramide |
- |
- |
1 |
1.00 |
||||||||||
|
FAVI |
- |
- |
- |
- |
- |
- |
- |
Quinidine |
- |
- |
4 |
4.00 |
||||||||||
|
INF-B |
- |
- |
- |
- |
- |
- |
- |
Flecainide |
- |
- |
4 |
4.00 |
||||||||||
|
LPV/r |
- |
- |
- |
- |
- |
- |
- |
Amiodarone |
- |
- |
1 |
1.03 |
||||||||||
|
LPV/r |
- |
- |
- |
- |
- |
- |
- |
Dofetilide |
- |
- |
1 |
1.03 |
||||||||||
|
TCZ |
- |
- |
- |
- |
- |
- |
- |
Bepridil |
- |
- |
4 |
3.89 |
||||||||||
|
INF-B |
- |
- |
- |
- |
- |
- |
- |
- |
Fosinopril |
- |
4 |
4.00 |
||||||||||
|
LPV/r |
- |
- |
- |
- |
- |
- |
- |
- |
Ramipril |
- |
4 |
3.99 |
||||||||||
|
LPV/r |
- |
- |
- |
- |
- |
- |
- |
- |
Trandolapril |
- |
4 |
3.99 |
||||||||||
|
RBV |
- |
- |
- |
- |
- |
- |
- |
- |
Ramipril |
- |
4 |
4.00 |
||||||||||
|
TCZ |
- |
- |
- |
- |
- |
- |
- |
- |
Trandolapril |
- |
4 |
4.00 |
||||||||||
|
HCLQ |
- |
- |
- |
- |
- |
- |
- |
- |
- |
Azathioprine |
2 |
2.04 |
||||||||||
|
HCLQ |
- |
- |
- |
- |
- |
- |
- |
- |
- |
Belatacept |
4 |
4.00 |
||||||||||
|
RDV |
- |
- |
- |
- |
- |
- |
- |
- |
- |
Mycophenolate |
4 |
4.00 |
||||||||||
|
RDV |
- |
- |
- |
- |
- |
- |
- |
- |
- |
Tacrolimus |
4 |
4.00 |
||||||||||
|
RBV |
- |
- |
- |
- |
- |
- |
- |
- |
- |
Basiliximab |
4 |
4.00 |
||||||||||
|
TCZ |
- |
- |
- |
- |
- |
- |
- |
- |
- |
Adalimumab |
1 |
2.04 |
||||||||||
|
TCZ |
- |
- |
- |
- |
- |
- |
- |
- |
- |
Sirolimus |
3 |
3.09 |
||||||||||